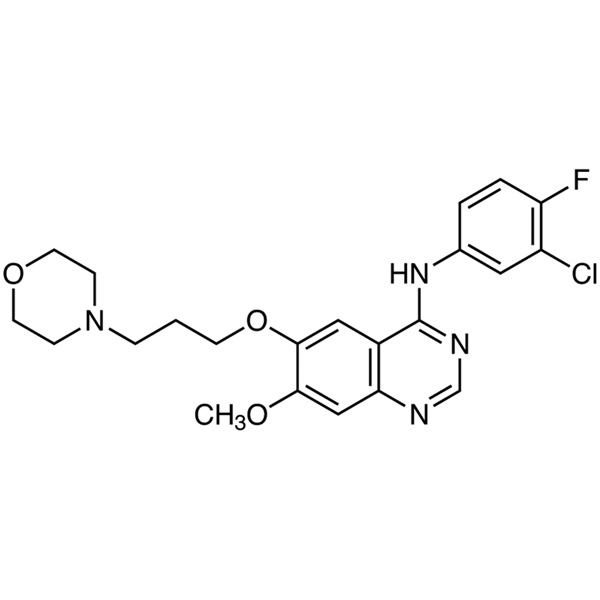
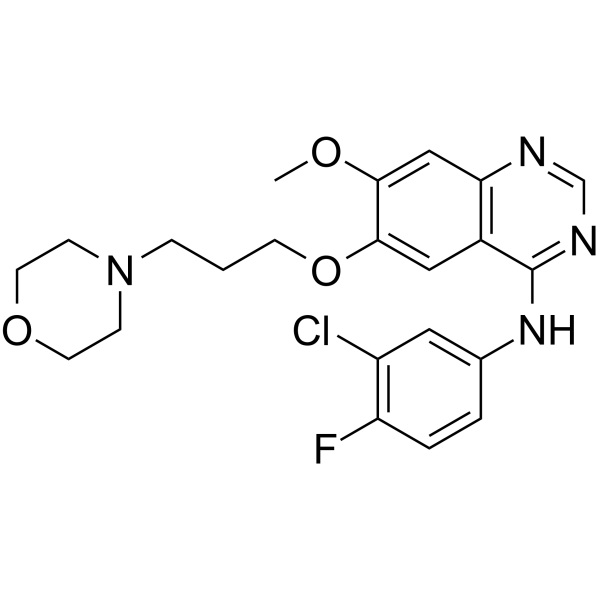
Gefitinib CAS 184475-35-2 Reinheit >99,5 % (HPLC)
Shanghai Ruifu Chemical Co., Ltd. ist der führende Hersteller von Gefitinib (CAS: 184475-35-2) mit hoher Qualität. Ruifu Chemical bietet weltweite Lieferung, wettbewerbsfähige Preise, exzellenten Service sowie die Verfügbarkeit kleiner und großer Mengen. Kaufen Sie Gefitinib und Zwischenprodukte, Bitte kontaktieren Sie: alvin@ruifuchem.com
| Chemischer Name | Gefitinib |
| Synonyme | Freie Base von Gefitinib; Iressa; ZD1839; ZD-1839; N-(3-Chlor-4-Fluorphenyl)-7-Methoxy-6-(3-Morpholinopropoxy)chinazolin-4-Amin; N-(3-Chlor-4-Fluorphenyl)-7-Methoxy-6-[3-(4-Morpholinyl)propoxy]-4-Chinazolinamin |
| Lagerstatus | Auf Lager, kommerzielle Produktion |
| CAS-Nummer | 184475-35-2 |
| Molekulare Formel | C22H24ClFN4O3 |
| Molekulargewicht | 446,91 g/mol |
| Schmelzpunkt | 194,0 bis 198,0℃ |
| Dichte | 1,322 ± 0,06 g/cm3 |
| Löslichkeit | Unlöslich in Wasser. Löslich in DMSO |
| Lagertemp. | Raumtemperatur |
| Versand | Ambiente |
| Echtheitszertifikat und Sicherheitsdatenblatt | Verfügbar |
| Herkunft | Shanghai, China |
| Produktkategorien | API (aktiver pharmazeutischer Inhaltsstoff) |
| Marke | Ruifu Chemical |
| Artikel | Inspektionsstandards | Ergebnisse |
| Aussehen | Weißes bis cremefarbenes Pulver | Entspricht |
| Verlust beim Trocknen | <0,50 % | 0,13 % |
| Rückstände bei der Zündung | <0,20 % | 0,06 % |
| Einzelne Verunreinigung | <0,10 % | 0,09 % |
| Gesamtverunreinigungen | <0,50 % | 0,20 % |
| Schwermetalle (Pb) | ≤10 ppm | <10 ppm |
| Gefitinib Reinheit | >99,5 % (HPLC) | 99,80 % |
| Infrarotspektrum | Im Einklang mit der Struktur | Entspricht |
| 1H-NMR-Spektrum | Im Einklang mit der Struktur | Entspricht |
| Fazit | Das Produkt wurde getestet und entspricht den angegebenen Spezifikationen | |
Paket: Fluorierte Flasche, Aluminiumfolienbeutel, 25 kg/Kartontrommel oder nach Kundenwunsch.
Lagerbedingungen: Halten Sie den Behälter fest verschlossen und lagern Sie ihn in einem kühlen, trockenen und gut belüfteten Lager, entfernt von unverträglichen Substanzen. Vor Licht und Feuchtigkeit schützen.
Versand:Lieferung weltweit per Luftfracht, per FedEx / DHL Express. Sorgen Sie für eine schnelle und zuverlässige Lieferung.
Nicht zur Anwendung beim Menschen geeignet. Nicht zur Verwendung in der Diagnostik oder Therapie geeignet. Nur für In-vitro-Forschungszwecke.
Keines der Produkte wird in Länder geliefert, in denen dies im Widerspruch zu den bestehenden Patenten stehen könnte. Die letzte Verantwortung liegt jedoch beim Käufer.
Wie kaufe ich? Bitte kontaktieren Sie unsDr. Alvin Huang: sales@ruifuchem.com oder alvin@ruifuchem.com
15 Jahre Erfahrung?Wir verfügen über mehr als 15 Jahre Erfahrung in der Herstellung und dem Export einer breiten Palette hochwertiger pharmazeutischer Zwischenprodukte oder Feinchemikalien.
Hauptmärkte? Verkauf auf dem Inlandsmarkt, Nordamerika, Europa, Indien, Korea, Japan, Australien usw.
Vorteile? Überlegene Qualität, erschwinglicher Preis, professionelle Dienstleistungen und technischer Support, schnelle Lieferung.
Qualität Sicherheit? Strenges Qualitätskontrollsystem. Zu den professionellen Analysegeräten gehören NMR, LC-MS, GC, HPLC, ICP-MS, UV, IR, OR, K.F, ROI, LOD, MP, Klarheit, Löslichkeit, mikrobieller Grenztest usw.
Proben? Bei den meisten Produkten werden kostenlose Muster zur Qualitätsbewertung bereitgestellt. Die Versandkosten müssen vom Kunden getragen werden.
Fabrikaudit? Werksaudit willkommen. Bitte vereinbaren Sie vorab einen Termin.
Mindestbestellmenge? Kein MOQ. Eine kleine Bestellung ist akzeptabel.
Lieferzeit? Wenn der Artikel vorrätig ist, ist die Lieferung innerhalb von drei Tagen garantiert.
Transport? Per Express (FedEx, DHL), auf dem Luftweg, auf dem Seeweg.
Dokumente? Kundendienst: COA, MOA, ROS, MSDS usw. können bereitgestellt werden.
Kundenspezifische Synthese? Kann maßgeschneiderte Synthesedienste anbieten, die Ihren Forschungsanforderungen am besten entsprechen.
Zahlungsbedingungen? Die Proforma-Rechnung wird Ihnen erst nach der Auftragsbestätigung zugesandt, unter Beifügung unserer Bankdaten. Zahlung per T/T (Telex-Überweisung), PayPal, Western Union usw.
| Sicherheitsbeschreibung | 24/25 - Kontakt mit Haut und Augen vermeiden. |
| HS-Code | 2934999099 |
Gefitinib (CAS: 184475-35-2) ist ein hochspezifisches, gegen Tumore gerichtetes therapeutisches Medikament, das von AstraZeneca, Großbritannien, entwickelt wurde. Es ist das erste molekular zielgerichtete Medikament zur Behandlung von nichtkleinzelligem Lungenkrebs. Es wirkt durch selektive Hemmung des Signaltransduktionswegs der Tyrosinkinase des epidermalen Wachstumsfaktorrezeptors (EGFR-TK). Der epidermale Wachstumsfaktor (EGF) ist ein Polypeptid mit einer relativen Molekülmasse von 6,45 × 103, das sich mit dem epidermalen Wachstumsfaktorrezeptor (EGFR) auf der Zielzellmembran verbinden kann, um biologische Wirkungen hervorzurufen. EGFR ist ein Rezeptor vom Typ Tyrosinkinase (TK). Wenn es an EGF bindet, kann es die TK-Aktivierung im Empfängerkörper fördern, was zur Autophosphorylierung von Rezeptortyrosinresten führt, wodurch kontinuierliche Teilungssignale an die Zellen gesendet werden, was zu Zellproliferation und -differenzierung führt. EGFR ist im menschlichen Gewebe reichlich vorhanden und wird in bösartigen Tumoren stark exprimiert. Durch die Blockierung des EGFR-Signalwegs auf der Zelloberfläche hemmt Gefitinib das Tumorwachstum, die Metastasierung und die Angiogenese und kann die Apoptose von Tumorzellen induzieren. Im August 2002 wurde Gefitinib erstmals in Japan als Erstlinientherapie bei nichtkleinzelligem Lungenkrebs unter dem Handelsnamen Iressa vermarktet. Im Mai 2003 genehmigte die US-amerikanische Food and Drug Administration Gefitinib als Monotherapie der dritten Wahl für Patienten mit fortgeschrittenem nichtkleinzelligem Lungenkrebs, bei denen platinbasierte Krebsmedikamente und eine Docetaxel-Chemotherapie wirkungslos waren. Derzeit ist es in Australien, Japan, Argentinien, Singapur und Südkorea für die Behandlung von fortgeschrittenem nichtkleinzelligem Lungenkrebs zugelassen. Am 28. Februar 2005 hat die chinesische Lebensmittel- und Arzneimittelbehörde Gefitinib für die Behandlung von lokal fortgeschrittenem oder metastasiertem nicht-kleinzelligem Lungenkrebs (NSCLC) zugelassen, der zuvor eine Chemotherapie erhalten hatte. Es ist derzeit nicht als Erstlinientherapie bei fortgeschrittenem NSCLC zugelassen. Am 1. Juli 2009 hat die Europäische Arzneimittel-Agentur Gefitinib offiziell für die Erstlinien-, Zweitlinien- und Drittlinienbehandlung von lokal fortgeschrittenem oder metastasiertem nichtkleinzelligem Lungenkrebs mit EGFR-Genmutationen bei Erwachsenen zugelassen.