Ceftarolin Fosamil 7-Position Seitenkette CAS 75028-24-9 Reinheit: ≥99,0 % (HPLC)
Herstellerversorgung mit hoher Reinheit und stabiler Qualität
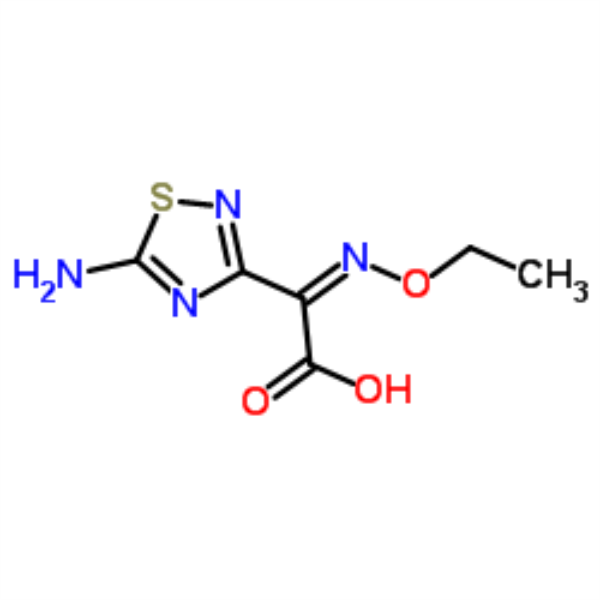
Chemischer Name: (Z)-2-(5-Amino-1,2,4-thiadiazol-3-yl)-2-(ethoxyimino)essigsäure
CAS: 75028-24-9
| Chemischer Name | (Z)-2-(5-Amino-1,2,4-thiadiazol-3-yl)-2-(ethoxyimino)essigsäure |
| Synonyme | Ceftarolin Fosamil 7-Position Seitenkette; ATDE |
| CAS-Nummer | 75028-24-9 |
| CAT-Nummer | RF-PI559 |
| Lagerstatus | Auf Lager, Produktionsmaßstab bis zu Tonnen |
| Molekulare Formel | C6H8N4O3S |
| Molekulargewicht | 216.22 |
| Marke | Ruifu Chemical |
| Artikel | Spezifikationen |
| Aussehen | Weißes bis hellgelbes kristallines Pulver |
| Reinheit / Analysemethode | ≥99,0 % (HPLC) |
| Feuchtigkeit (K.F) | ≤0,50 % |
| Einzelne Verunreinigung | ≤0,50 % |
| Gesamtverunreinigungen | ≤1,0 % |
| Teststandard | Unternehmensstandard |
| Nutzung | Zwischenprodukt von Ceftarolin Fosamil (TAK-599), einem Cephalosporin-Derivat |
Paket: Flasche, Aluminiumfolienbeutel, 25 kg/Kartontrommel oder nach Kundenwunsch.
Lagerbedingungen:In verschlossenen Behältern kühl und trocken lagern; Vor Licht und Feuchtigkeit schützen.


(Z)-2-(5-Amino-1,2,4-thiadiazol-3-yl)-2-(ethoxyimino)essigsäure (CAS: 75028-24-9) ist ein wichtiges Zwischenprodukt für die Herstellung von Ceftarolin Fosamil (TAK-599). Ceftarolinfosamil ist ein Cephalosporin mit Wirkung gegen grampositive Krankheitserreger, einschließlich Methicillin-resistentem Staphylococcus aureus (MRSA). Ceftarolin Fosamil ist ein Prodrug von Ceftarolin. Es wird von Forest Laboratories unter einer Lizenz von Takeda entwickelt. Am 29. Oktober 2010 erhielt es von der US-amerikanischen Food and Drug Administration (FDA) die Zulassung zur Behandlung von ambulant erworbener bakterieller Lungenentzündung und akuten bakteriellen Hautinfektionen.