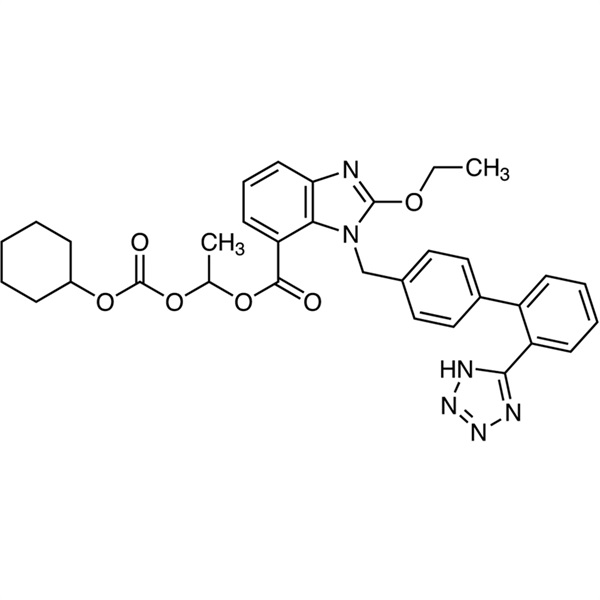
Candesartan Cilexetil CAS 145040-37-5 Gehalt 99,0–101,0 % API EP-Standard
Ruifu Chemical ist der führende Anbieter von Candesartan Cilexetil (CAS: 145040-37-5) mit hoher Qualität und kann den EP-Standard erfüllen. Ruifu liefert seit mehr als 15 Jahren APIs und pharmazeutische Zwischenprodukte.
Ruifu Chemical bietet weltweite Lieferung, wettbewerbsfähige Preise und exzellenten Service.
Wenn Sie Candesartan Cilexetil und seine Zwischenprodukte kaufen möchten, kontaktieren Sie uns bitte per E-Mail: alvin@ruifuchem.com
Ruifu Chemical Supply Candesartan Cilexetil Intermediate mit hoher Reinheit
Candesartan Cilexetil CAS 145040-37-5
Candesartan CAS 139481-59-7
1-Chlorethylcyclohexylcarbonat CAS 99464-83-2
Candesartan Cilexetil Intermediate Eethyl Ester C6 CAS 139481-41-7
Candesartan-Cilexetil-Zwischenprodukt CAS 139481-44-0
Trityl Candesartan Cilexetil CAS 170791-09-0
| Chemischer Name | Candesartan Cilexetil |
| Synonyme | TCV-116; 1-(((Cyclohexyloxy)carbonyl)oxy)ethyl 1-((2'-(1H-tetrazol-5-yl)-[1,1'-biphenyl]-4-yl)methyl)-2-ethoxy-1H-benzo[d]imidazol-7-Carboxylat |
| CAS-Nummer | 145040-37-5 |
| Lagerstatus | Auf Lager, Produktionsmaßstab bis zu Tonnen |
| Molekulare Formel | C33H34N6O6 |
| Molekulargewicht | 610,66 |
| Dichte | 1,37 ± 0,10 g/cm3 |
| Schmelzpunkt | 168,0-170,0℃ |
| Echtheitszertifikat und Sicherheitsdatenblatt | Verfügbar |
| Lagerbedingungen | 2-8℃ |
| Empfindlich | Empfindlich gegenüber Hitze |
| Herkunft des Produkts | Shanghai, China |
| Produktkategorien | API (aktiver pharmazeutischer Inhaltsstoff) |
| Marke | Ruifu Chemical |
| Artikel | Spezifikationen | Ergebnisse |
| Aussehen | Weißes oder fast weißes Pulver | Weißes Pulver |
| Identifikation-IR | Entspricht dem Referenzspektrum | Konform |
| Identifikation- UV | Maximale Absorptionen bei 254 nm, minimale Absorption bei 242 nm | Konform |
| Wasser (K.F) | ≤0,30 % | 0,19 % |
| Restlösungsmittel | ||
| Methanol | ≤3000 ppm | Nicht erkannt |
| Ethanol | ≤5000 ppm | Nicht erkannt |
| Ethylether | ≤5000 ppm | 62 Seiten pro Minute |
| Aceton | ≤5000 ppm | 505 ppm |
| Ethylacetat | ≤5000 ppm | Nicht erkannt |
| Dichlormethan | ≤600 ppm | Nicht erkannt |
| Dimethylformamid | ≤880 ppm | Nicht erkannt |
| Verwandte Substanzen | ||
| Verunreinigung A | ≤0,15 % | 0,04 % |
| Verunreinigung B | ≤0,30 % | 0,03 % |
| Verunreinigung F | ≤0,20 % | 0,02 % |
| Verunreinigung G | ≤0,20 % | 0,04 % |
| Verunreinigung H | ≤0,15 % | Nicht erkannt |
| Andere individuelle Verunreinigungen | ≤0,10 % | 0,04 % |
| Gesamtverunreinigungen | ≤0,60 % | 0,23 % |
| Sulfatasche | ≤0,10 % | 0,07 % |
| Schwermetalle | ≤10 ppm | <10 ppm |
| Gehalt (getrocknete Substanz) | 99,0–101,0 % | 99,9 % |
| Teststandard | EP-Standard | Konform |
Paket: Flasche, Aluminiumfolienbeutel, 25 kg/Kartontrommel oder nach Kundenwunsch.
Lagerbedingungen: Halten Sie den Behälter fest verschlossen. In einem kühlen, trockenen (2-8℃) und gut belüfteten Lager, entfernt von unverträglichen Substanzen, lagern. Von Sonnenlicht fernhalten; Vermeiden Sie Feuer und Wärmequellen. Feuchtigkeit vermeiden.
Versand: Lieferung in die ganze Welt per Flugzeug, auf dem Seeweg, per FedEx / DHL Express. Sorgen Sie für eine schnelle und zuverlässige Lieferung.

Risikocodes
R20/21/22 - Gesundheitsschädlich beim Einatmen, bei Berührung mit der Haut und beim Verschlucken.
R36/37/38 - Reizt Augen, Atemwege und Haut.
R50 - Sehr giftig für Wasserorganismen
R48/20 -
R61 - Kann dem ungeborenen Kind schaden
Sicherheitsbeschreibung
S26 - Bei Augenkontakt sofort mit viel Wasser ausspülen und ärztlichen Rat einholen.
S36 - Tragen Sie geeignete Schutzkleidung.
S61 - Freisetzung in die Umwelt vermeiden. Besondere Hinweise/Sicherheitsdatenblätter beachten.
S45 - Bei Unfall oder Unwohlsein sofort ärztlichen Rat einholen (wenn möglich dieses Etikett vorzeigen).
S53 - Exposition vermeiden - Vor Gebrauch besondere Anweisungen einholen.
WGK Deutschland 3
RTECS DD6672500
HS-Code 2933990099
Candesartan Cilexetil (TCV-116) (CAS: 145040-37-5) ist ein Angiotensin-II-Rezeptor-Antagonist mit einem IC50-Wert von 0,26 nM, der zur Behandlung von Bluthochdruck eingesetzt wird. Candesartan ist ein Angiotensin-Rezeptorblocker (ARB), der allein oder zusammen mit anderen Wirkstoffen zur Behandlung von Bluthochdruck eingesetzt werden kann. Es wird oral als Prodrug Candesartan Cilexetil verabreicht, das während der Absorption im Magen-Darm-Trakt schnell in seinen aktiven Metaboliten Candesartan umgewandelt wird. Candesartan senkt den Blutdruck, indem es das Renin-Angiotensin-Aldosteron-System (RAAS) antagonisiert. Es konkurriert mit Angiotensin II um die Bindung an den Typ-1-Angiotensin-II-Rezeptor (AT1)-Subtyp und verhindert die blutdrucksteigernde Wirkung von Angiotensin II. Im Gegensatz zu Angiotensin-Converting-Enzym-Hemmern (ACE-Hemmern) haben ARBs nicht die nachteilige Wirkung von trockenem Husten. Candesartan kann zur Behandlung von Bluthochdruck, isolierter systolischer Hypertonie, linksventrikulärer Hypertrophie und diabetischer Nephropathie eingesetzt werden. Es kann auch als alternatives Mittel zur Behandlung von Herzinsuffizienz, systolischer Dysfunktion, Myokardinfarkt und koronarer Herzkrankheit eingesetzt werden.
CANDESARTAN CILEXETIL
Candesartanum cilexetili
C33H34N6O6 Herr 611
[145040-37-5]
DEFINITION
(1RS)-1-[[(Cyclohexyloxy)carbonyl]oxy]ethyl
2-Ethoxy-1-[[2′-(1H-tetrazol-5-yl)biphenyl-4-yl]methyl]-1H-benzimidazol-7-carboxylat.
Inhalt: 99,0 Prozent bis 101,0 Prozent (wasserfreie Substanz).
PRODUKTION
Da N-Nitrosamine als wahrscheinlich krebserregend für den Menschen eingestuft werden, sollte ihr Vorkommen in Candesartan Cilexetil vermieden oder so weit wie möglich begrenzt werden. Aus diesem Grund wird von Herstellern von Candesartancilexetil für den menschlichen Gebrauch erwartet, dass sie während ihres Herstellungsprozesses eine Bewertung des Risikos der Bildung und Kontamination von N-Nitrosamin durchführen; Wenn bei dieser Bewertung ein potenzielles Risiko festgestellt wird, sollte der Herstellungsprozess geändert werden, um die Kontamination zu minimieren, und eine Kontrollstrategie zur Erkennung und Kontrolle von N-Nitrosamin-Verunreinigungen in Candesartan Cilexetil implementiert werden. Das allgemeine Kapitel 2.5.42. Zur Unterstützung der Hersteller steht N-Nitrosamine in Wirkstoffen zur Verfügung.
CHARAKTERE
Aussehen: weißes oder fast weißes Pulver.
Löslichkeit: praktisch unlöslich in Wasser, frei löslich in Methylenchlorid und schwer löslich in wasserfreiem Ethanol.
Es zeigt Polymorphismus (5.9).
IDENTIFIZIERUNG
Infrarot-Absorptionsspektrophotometrie (2.2.24).
Vergleich: Candesartan Cilexetil CRS.
Wenn die erhaltenen Spektren Unterschiede aufweisen, lösen Sie die zu untersuchende Substanz und die Referenzsubstanz getrennt in wasserfreiem Ethanol R, verdampfen Sie zur Trockne und nehmen Sie mit den Rückständen neue Spektren auf.
TESTS
Verwandte Substanzen. Flüssigkeitschromatographie (2.2.29). Bereiten Sie die Lösungen unmittelbar vor der Verwendung vor.
Lösungsmittelmischung: Wasser R, Acetonitril R (40:60 V/V).
Testlösung. Lösen Sie 20 mg der zu untersuchenden Substanz in 50,0 ml des Lösungsmittelgemisches.
Referenzlösung (a). Verdünnen Sie 1,0 ml der Testlösung mit der Lösungsmittelmischung auf 100,0 ml. Verdünnen Sie 1,0 ml dieser Lösung mit der Lösungsmittelmischung auf 10,0 ml.
Referenzlösung (b). Lösen Sie 5 mg Candesartan Cilexetil für Systemeignung CRS (enthält die Verunreinigungen A, B und F) in der Lösungsmittelmischung und verdünnen Sie es mit der Lösungsmittelmischung auf 10 ml.
Referenzlösung (c). Lösen Sie 2,5 mg Candesartan Cilexetil zur Peakidentifikation CRS (enthält die Verunreinigungen G und H) in der Lösungsmittelmischung und verdünnen Sie es mit der Lösungsmittelmischung auf 5 ml.
Spalte:
- Größe: l = 0,15 m, Ø = 3,9 mm;
- stationäre Phase: endverkapptes Octadecylsilyl-Kieselgel für
Chromatographie R (4 μm).
Mobile Phase:
- mobile Phase A: Eisessig R, Wasser für
Chromatographie R, Acetonitril R (1:43:57 V/V/V);
- mobile Phase B: Eisessig R, Wasser für
Chromatographie R, Acetonitril R (1:10:90 V/V/V);
Zeit (Min.) Mobile Phase A (Prozent V/V) Mobile Phase B (Prozent V/V)
0 - 3 100 0
3 - 33 100 → 0 0 → 100
33 - 40 0 100
Flussrate: 0,8 ml/min.
Nachweis: Spektrophotometer bei 254 nm.
Injektion: 10 μL.
Identifizierung von Verunreinigungen: Verwenden Sie das mit Candesartancilexetil gelieferte Chromatogramm für die Systemeignung (CRS) und das mit der Referenzlösung (b) erhaltene Chromatogramm, um die Peaks aufgrund der Verunreinigungen A, B und F zu identifizieren. Verwenden Sie das mit Candesartan Cilexetil gelieferte Chromatogramm zur Peakidentifizierung (CRS) und das mit der Referenzlösung (c) erhaltene Chromatogramm zur Identifizierung der Peaks aufgrund der Verunreinigungen G und H.
Relative Retention in Bezug auf Candesartancilexetil
(Retentionszeit = ca. 11 Minuten): Verunreinigung G = ca. 0,2;
Verunreinigung A = ungefähr 0,4; Verunreinigung B = ungefähr 0,5;
Verunreinigung F = ungefähr 2,0; Verunreinigung H = ungefähr 3,5.
Systemeignung: Referenzlösung (b):
- Auflösung: mindestens 4,0 zwischen den Peaks aufgrund der Verunreinigungen A und B.
Grenzen:
- Korrekturfaktoren: Zur Berechnung des Gehalts multiplizieren Sie die Peakflächen der folgenden Verunreinigungen mit dem entsprechenden Korrekturfaktor: Verunreinigungen A und G = 0,7;
Verunreinigung H = 1,6;
- Verunreinigung B: nicht mehr als das Dreifache der Fläche des Hauptpeaks im Chromatogramm, das mit der Referenzlösung (a) erhalten wurde (0,3 Prozent);
- Verunreinigungen F, G: für jede Verunreinigung nicht mehr als das Doppelte der Fläche des Hauptpeaks im Chromatogramm, das mit der Referenzlösung (a) erhalten wurde (0,2 Prozent);
- Verunreinigungen A, H: für jede Verunreinigung nicht mehr als das 1,5-fache der Fläche des Hauptpeaks im Chromatogramm, das mit der Referenzlösung (a) erhalten wurde (0,15 Prozent);
- nicht spezifizierte Verunreinigungen: für jede Verunreinigung nicht mehr als die Fläche des Hauptpeaks im Chromatogramm, das mit der Referenzlösung (a) erhalten wurde (0,10 Prozent);
- insgesamt: nicht mehr als das Sechsfache der Fläche des Hauptpeaks im Chromatogramm, das mit der Referenzlösung (a) erhalten wurde (0,6 Prozent);
- Grenzwert außer Acht lassen: 0,5-fache Fläche des Hauptpeaks im Chromatogramm, das mit der Referenzlösung (a) erhalten wurde (0,05 Prozent).
Wasser (2.5.32): maximal 0,3 Prozent, bestimmt auf 60,0 mg.
Sulfatasche (2.4.14): maximal 0,1 Prozent, bestimmt auf 1,0 g.
TEST
0,500 g in 60 ml Eisessig R auflösen. Sofort mit 0,1 M Perchlorsäure titrieren und dabei den Endpunkt potentiometrisch (2.2.20) am 1. Wendepunkt bestimmen.
1 ml 0,1 M Perchlorsäure entspricht 61,1 mg C33H34N6O6.
VERUNREINIGUNGEN
Spezifizierte Verunreinigungen: A, B, F, G, H.
Andere nachweisbare Verunreinigungen (die folgenden Stoffe würden, wenn sie in ausreichender Menge vorhanden wären, durch einen der Tests in der Monographie nachgewiesen werden. Sie sind durch das allgemeine Akzeptanzkriterium für andere/nicht spezifizierte Verunreinigungen und/oder durch die allgemeine Monographie Stoffe für pharmazeutische Zwecke (2034) begrenzt. Es ist daher nicht erforderlich, diese Verunreinigungen zum Nachweis der Konformität zu identifizieren. Siehe auch 5.10. Kontrolle von Verunreinigungen in Stoffen für pharmazeutische Zwecke): C, D, E, I.
A. Ethyl 2-ethoxy-1-[[2′-(1H-tetrazol-5-yl)biphenyl-4-yl]methyl]-1H-benzimidazol-7-carboxylat,
B. (1RS)-1-[[(Cyclohexyloxy)carbonyl]oxy]ethyl 2-oxo-3-[[2′-(1H-tetrazol-5-yl)biphenyl-4-yl]methyl]-2,3-dihydro-1H-benzimidazol-4-carboxylat,
C. (1RS)-1-[[(Cyclohexyloxy)carbonyl]oxy]ethyl 3-[[2′-(1-ethyl-1H-tetrazol-5-yl)biphenyl-4-yl]methyl]-2-oxo-2,3-dihydro-1H-benzimidazol-4-carboxylat,
D. (1RS)-1-[[(Cyclohexyloxy)carbonyl]oxy]ethyl 3-[[2′-(2-ethyl-2H-tetrazol-5-yl)biphenyl-4-yl]methyl]-2-oxo-2,3-dihydro-1H-benzimidazol-4-carboxylat,
E. (1RS)-1-[[(Cyclohexyloxy)carbonyl]oxy]ethyl 2-ethoxy-1-[[2′-(1-ethyl-1H-tetrazol-5-yl)biphenyl-4-yl]methyl]-1H-benzimidazol-7-carboxylat,
F. (1RS)-1-[[(Cyclohexyloxy)carbonyl]oxy]ethyl 2-ethoxy-1-[[2′-(2-ethyl-2H-tetrazol-5-yl)biphenyl-4-yl]methyl]-1H-benzimidazol-7-carboxylat,
G. 2-Ethoxy-1-[[2′-(1H-Tetrazol-5-yl)biphenyl-4-yl]methyl]-1H-Benzimidazol-7-Carbonsäure (Candesartan),
H. (1RS)-1-[[(Cyclohexyloxy)carbonyl]oxy]ethyl 2-ethoxy-1-[[2′-[1-(triphenylmethyl)-1H-tetrazol-5-yl]biphenyl-4-yl]methyl]-1H-benzimidazol-7-carboxylat
(N-Tritylcandesartan),
I. Methyl-2-ethoxy-1-[[2′-(1H-tetrazol-5-yl)biphenyl-4-yl]methyl]-1H-benzimidazol-7-carboxylat.