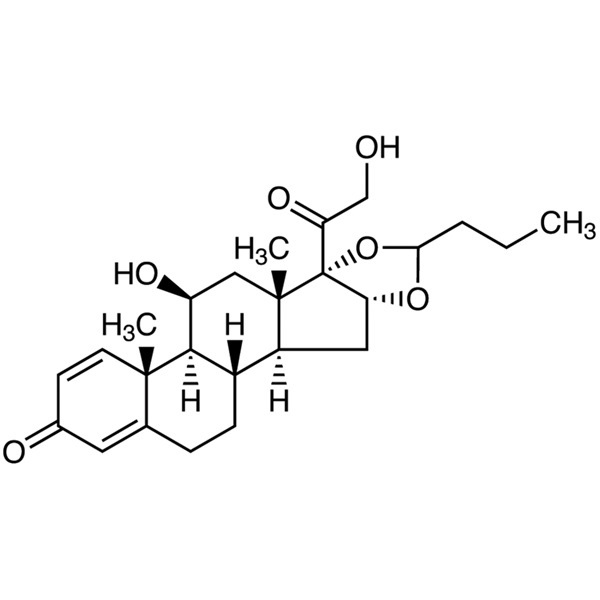
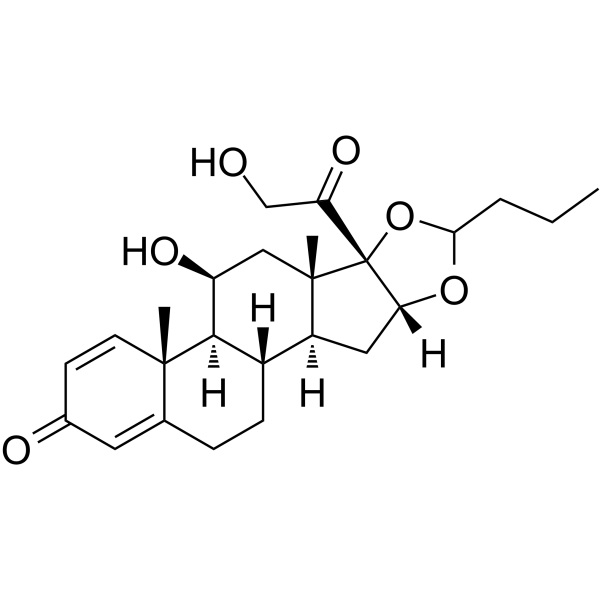
Budesonid CAS 51333-22-3 Gehalt 98,0–102,0 %
Shanghai Ruifu Chemical Co., Ltd. ist der führende Hersteller von Budesonid (CAS: 51333-22-3) mit hoher Qualität. Ruifu Chemical bietet weltweite Lieferung, wettbewerbsfähige Preise, exzellenten Service sowie die Verfügbarkeit kleiner und großer Mengen. Kaufen Sie Budesonid, Bitte kontaktieren Sie: alvin@ruifuchem.com
| Chemischer Name | Budesonid |
| Synonyme | (+)-16α,17α-Butylidendioxy-11β,21-Dihydroxy-1,4-Pregnadien-3,20-Dion; 16,17-Butylidenbis(oxy)-11,21-Dihydroxypregna-1,4-Dien-3,20-Dion; Rhinocort; Pulmicort; Entocort; Symbicort |
| Lagerstatus | Auf Lager, kommerzielle Produktion |
| CAS-Nummer | 51333-22-3 |
| Molekulare Formel | C25H34O6 |
| Molekulargewicht | 430,54 g/mol |
| Schmelzpunkt | 221,0~232,0℃ |
| Löslichkeit | Unlöslich in Wasser. Löslich in Chloroform, Methanol. Leicht löslich in Ethanol und Aceton. Sehr schwer löslich in Dichlormethan und Ether |
| Echtheitszertifikat und Sicherheitsdatenblatt | Verfügbar |
| Herkunft des Produkts | Shanghai, China |
| Produktkategorien | API (aktiver pharmazeutischer Inhaltsstoff) |
| Achtung | Nicht für den menschlichen Gebrauch bestimmt. Nur für Forschungszwecke. |
| Marke | Ruifu Chemical |
| Artikel | Spezifikationen | Ergebnisse |
| Aussehen | Weißes bis cremefarbenes kristallines Pulver | Weißes kristallines Pulver |
| Budesonid-Assay | 98,0–102,0 % | 98,7 % |
| Verlust beim Trocknen | <0,30 % | 0,19 % |
| Jede einzelne Verunreinigung | <0,20 % | <0,20 % |
| Epimer A | 40,0~51,0 % | 47,29 % |
| Methanol | <0,10 % | 0,005 % |
| Infrarotspektrum | Im Einklang mit der Struktur | Entspricht |
| 1H-NMR-Spektrum | Im Einklang mit der Struktur | Entspricht |
| Fazit | Das Produkt wurde getestet und entspricht den angegebenen Spezifikationen | |
Paket: Flasche, Aluminiumfolienbeutel, 25 kg/Kartontrommel oder nach Kundenwunsch.
Lagerbedingungen: Halten Sie den Behälter fest verschlossen. In einem kühlen, trockenen (2~8℃) und gut belüfteten Lagerhaus, entfernt von unverträglichen Substanzen, lagern. Von Sonnenlicht fernhalten; Vermeiden Sie Feuer und Wärmequellen. Feuchtigkeit vermeiden.
Versand:Lieferung weltweit per Luftfracht, per FedEx / DHL Express. Sorgen Sie für eine schnelle und zuverlässige Lieferung.
Budesonid
C25H34O6 430,53
Pregna-1,4-dien-3,20-dion, 16,17-[1R-butylidenbis(oxy)]-11,21-dihydroxy und pregna-1,4-dien-3,20-dion,16,17-[1S-butylidenbis(oxy)]-11,21-dihydroxy;
(RS)-11,16,17,21-Tetrahydroxypregna-1,4-dien-3,20-dion cyclisches 16,17-acetal mit Butyraldehyd [51372-29-3; 51372-28-2; 51333-22-3].
DEFINITION
Ändern Sie den Text:
Budesonid ist eine Mischung aus zwei epimeren Formen, Epimer A(C-22S) und Epimer B(C-22R). Es enthält 40,0 % NLT (RB 1-Jun-2011) und 51,0 % NMT des Epimers A, und die Summe beider Epimere beträgt 98,0 % NLT und 102,0 % NMT von C25H34O6, berechnet auf der Trockenbasis.
[Hinweis-Schützen Sie alle Lösungen, die Budesonid enthalten, vor Licht.]
IDENTIFIZIERUNG
• A. Infrarotabsorption<197K>
• B. Ultraviolettabsorption<197U>
Probenlösung: 25 µg/ml
Medium: Methanol
Akzeptanzkriterien: Erfüllt die Anforderungen
TEST
Ändern Sie den Text:
• Vorgehensweise
Puffer: 3,17 mg/ml monobasisches Natriumphosphat und 0,23 mg/ml Phosphorsäure. Der pH-Wert beträgt 3,2 ± 0,1.
Mobile Phase: Acetonitril und Puffer (32:68)
Standardlösung: Eine Menge USP Budesonide RS in Acetonitril auflösen und quantitativ mit Puffer verdünnen, um eine Lösung mit einer Konzentration von 0,5 mg/ml zu erhalten, wobei der Anteil an Acetonitril in dieser Lösung auf NMT 30 % gehalten wird.
Probenlösung: 25 mg Budesonid in 15 ml Acetonitril in einem 50-ml-Messkolben auflösen und mit Puffer auf das Volumen verdünnen.
Chromatographisches System
(Siehe Chromatographie<621>, Systemeignung.)
Modus: LC
Detektor: UV 254 nm
Säule: 4,6 mm × 15 cm; 5-µm Packung L1
Flussrate: 1,5 ml/min
Injektionsgröße: 20 µL
Systemtauglichkeit
Beispiel: Standardlösung
[Hinweis-Die relative Retentionszeit für Epimer A beträgt 1,1 im Vergleich zu Epimer B.]
Eignungsanforderungen
Auflösung: NLT 1,5 zwischen den beiden Budesonid-Epimer-Peaks
Säuleneffizienz: NLT 5500 theoretische Böden, bestimmt aus dem Budesonid-Epimer-B-Peak
Analyse
Proben: Standardlösung und Musterlösung
Berechnen Sie den Prozentsatz an Epimer A (C25H34O6) in der eingenommenen Portion Budesonid:
Ergebnis = [rUA/(rUA + rUB)] × 100
rUA = Peakfläche von Epimer A aus der Probenlösung
rUB = Peakfläche von Epimer B aus der Probenlösung
Berechnen Sie den Prozentsatz von C25H34O6 in der eingenommenen Portion Budesonid:
Ergebnis = [(rUA + rUB)/(rSA + rSB)] × (CS/CU) × 100
rUA = Peakfläche von Epimer A aus der Probenlösung
rUB = Peakfläche von Epimer B aus der Probenlösung
rSA = Peakfläche von Epimer A aus der Standardlösung
rSB = Peakfläche von Epimer B aus der Standardlösung
CS = Konzentration von USP Budesonid RS in der Standardlösung (mg/ml)
CU = Konzentration von Budesonid in der Probenlösung (mg/ml)
Akzeptanzkriterien
Epimer A: 40,0 % (RB 1-Jun-2011) - 51,0 % auf Trockenbasis
Beide Epimere: 98,0 % - 102,0 % auf Trockenbasis
VERUNREINIGUNGEN
• Verfahren 1: Grenzwert von 21-Acetat von Budesonid
Puffer: 3,17 mg/ml monobasisches Natriumphosphat und 0,23 mg/ml Phosphorsäure. Der pH-Wert beträgt 3,2 ± 0,1.
Mobile Phase: Acetonitril und Puffer (45:55)
Standardlösung: Eine Menge USP Budesonide RS in Acetonitril auflösen und quantitativ mit Puffer verdünnen, um eine Lösung mit einer Konzentration von 0,5 mg/ml zu erhalten, wobei der Anteil an Acetonitril in dieser Lösung auf NMT 30 % gehalten wird.
Probenlösung: 25 mg Budesonid in 15 ml Acetonitril in einem 50-ml-Messkolben auflösen und mit Puffer auf das Volumen verdünnen.
Chromatographisches System
(Siehe Chromatographie<621>, Systemeignung.)
Modus: LC
Detektor: UV 254 nm
Säule: 4,6 mm × 15 cm; 5-µm Packung L1
Flussrate: 1,5 ml/min
Injektionsgröße: 20 µL
Systemtauglichkeit
Beispiel: Standardlösung
[Anmerkung-Die relativen Retentionszeiten für das erste eluierte Epimer des 21-Acetats von Budesonid, das zweite eluierte Epimer des 21-Acetats von Budesonid, das erste eluierte Epimer von Budesonid (Epimer B) und das zweite eluierte Epimer von Budesonid (Epimer A) betragen 3,1, 3,2, 1,0 und 1,1. bzw. ]
Eignungsanforderungen
Säuleneffizienz: NLT 5500 theoretische Böden, bestimmt aus dem Budesonid-Epimer-B-Peak
Analyse
Probe: Musterlösung
Berechnen Sie den Prozentsatz des 21-Acetats von Budesonid in der eingenommenen Portion Budesonid:
Ergebnis = (rT1/rT2) × 100
rT1 = Summe der Peakflächen für die beiden Epimere des 21-Acetats von Budesonid
rT2 = Summe der Peakflächen der beiden Budesonid-Peaks
Akzeptanzkriterien: NMT 0,10 % des 21-Acetats von Budesonid werden gefunden.
• Verfahren 2: Grenzwert von 11-Ketobudesonid
Puffer: 3,17 mg/ml monobasisches Natriumphosphat und 0,23 mg/ml Phosphorsäure. Der pH-Wert beträgt 3,2 ± 0,1.
Mobile Phase: Acetonitril, Isopropanol und Puffer (26:9:65)
Standardlösung: Eine Menge USP Budesonide RS in Acetonitril auflösen und quantitativ mit Puffer verdünnen, um eine Lösung mit einer Konzentration von 0,5 mg/ml zu erhalten, wobei der Anteil an Acetonitril in dieser Lösung auf NMT 30 % gehalten wird.
Probenlösung: 25 mg Budesonid in 15 ml Acetonitril in einem 50-ml-Messkolben auflösen und mit Puffer auf das Volumen verdünnen.
Chromatographisches System
(Siehe Chromatographie<621>, Systemeignung.)
Modus: LC
Detektor: UV 254 nm
Säule: 4,6 mm × 15 cm; 3,5 µm Packung L1
Säulentemperatur: 50
[Hinweis-Heizen Sie die mobile Phase auf 50 °C vor.]
Flussrate: 1,5 ml/min
Injektionsgröße: 20 µL
Systemtauglichkeit
Beispiel: Standardlösung
[Anmerkung-Die relativen Retentionszeiten für die beiden Epimere von 11-Ketobudesonid betragen 0,73 bzw. 0,78; Die relativen Retentionszeiten für 21-Dehydrobudesonid, 14,15-Dehydrobudesonid und das erste eluierte Epimer von Budesonid (Epimer B) betragen 0,68, 0,84 bzw. 1,0.]
Eignungsanforderungen
Säuleneffizienz: NLT 5500 theoretische Böden, bestimmt aus dem Budesonid-Epimer-B-Peak
Analyse
Probe: Musterlösung
Berechnen Sie den Prozentsatz von 11-Ketobudesonid in der eingenommenen Portion Budesonid:
Ergebnis = (rT1/rT2) × 100
rT1 = Summe der Peakflächen der beiden Ketobudesonid-Peaks
rT2 = Summe der Peakflächen der beiden Budesonid-Peaks
Akzeptanzkriterien: NMT 0,2 % von 11-Ketobudesonid wurden gefunden.
• Verfahren 3
Puffer: 3,17 mg/ml monobasisches Natriumphosphat und 0,23 mg/ml Phosphorsäure. Der pH-Wert beträgt 3,2 ± 0,1.
Mobile Phase: Acetonitril und Puffer (32:68)
Standardlösung: Eine Menge USP Budesonide RS in Acetonitril auflösen und quantitativ mit Puffer verdünnen, um eine Lösung mit einer Konzentration von 0,5 mg/ml zu erhalten, wobei der Anteil an Acetonitril in dieser Lösung auf NMT 30 % gehalten wird.
Probenlösung: 25 mg Budesonid in 15 ml Acetonitril in einem 50-ml-Messkolben auflösen und mit Puffer auf das Volumen verdünnen.
Chromatographisches System
(Siehe Chromatographie<621>, Systemeignung.)
Modus: LC
Detektor: UV 254 nm
Säule: 4,6 mm × 15 cm; 5-µm Packung L1
Flussrate: 1,5 ml/min
Injektionsgröße: 20 µL
Systemtauglichkeit
Beispiel: Standardlösung
Eignungsanforderungen
Säuleneffizienz: NLT 5500 theoretische Böden, bestimmt aus dem Budesonid-Epimer-B-Peak
Analyse
Probe: Musterlösung
Berechnen Sie den Prozentsatz jeder Verunreinigung in der eingenommenen Portion Budesonid:
Ergebnis = (rU/rT) × 100
rU = Peakfläche für jede Verunreinigung
rT = Summe der Flächen aller Peaks
Akzeptanzkriterien: Siehe Tabelle 1.
Tabelle 1 Name Relative Retentionszeit-Akzeptanzkriterien, NMT (%)
16-Hydroxyprednisolon 0,11 0,2
d-Homobudesonideb 0,36 0,10
21-Dehydrobudesonid (Epimere)c 0,61; 0,66 0,07d
14,15-Dehydrobudesonid 0,86 0,10
Gesamte spezifizierte Verunreinigungen - 0,4f
Jede andere individuelle Verunreinigung - 0,10
Gesamte nicht spezifizierte Verunreinigungen - 0,4
a 11,16,17,21-Tetrahydroxypregna-1,4-dien-3,20-dion.
b 16,17-[(1RS)-Butylidenbis(oxy)]-11-hydroxy-17-(hydroxymethyl)-d-homoandrosta-1,4-dien-3,17a-dion.
c 16,17-[(1RS)-Butylidenbis(oxy)]-11-hydroxy-3,20-dioxopregna-1,4-dien-21-al.
d Limit umfasst beide Epimere.
e 16,17-[(1RS)-Butylidenbis(oxy)]-11,21-dihydroxypregna-1,4,14-trien-3,20-dion.
f Die Gesamtzahl der angegebenen Verunreinigungen umfasst 11-Ketobudesonid, das im Test auf den Grenzwert von 11-Ketobudenosid erhalten wurde, und die oben aufgeführten Verunreinigungen.
SPEZIFISCHE TESTS
• Mikrobenzählungstests<61>und Tests für bestimmte Mikroorganismen<62>: Die gesamte aerobe Mikrobenzahl beträgt NMT 103 KBE/g, und die Gesamtzahl an Schimmelpilzen und Hefen beträgt NMT 102 KBE/g.
• Trocknungsverlust<731>: Trocknen Sie eine Probe bei 105 bis zur Gewichtskonstanz: Sie verliert 0,3 % ihres Gewichts an NMT.
ZUSÄTZLICHE ANFORDERUNGEN
• Verpackung und Lagerung: In dichten, lichtbeständigen Behältern aufbewahren. Bei kontrollierter Raumtemperatur lagern.
• USP-Referenzstandards<11>
USP Budesonid RS
Wie kaufe ich? Bitte kontaktieren Sie unsDr. Alvin Huang: sales@ruifuchem.com oder alvin@ruifuchem.com
15 Jahre Erfahrung?Wir verfügen über mehr als 15 Jahre Erfahrung in der Herstellung und dem Export einer breiten Palette hochwertiger pharmazeutischer Zwischenprodukte oder Feinchemikalien.
Hauptmärkte? Verkauf auf dem Inlandsmarkt, Nordamerika, Europa, Indien, Korea, Japan, Australien usw.
Vorteile? Überlegene Qualität, erschwinglicher Preis, professionelle Dienstleistungen und technischer Support, schnelle Lieferung.
Qualität Sicherheit? Strenges Qualitätskontrollsystem. Zu den professionellen Analysegeräten gehören NMR, LC-MS, GC, HPLC, ICP-MS, UV, IR, OR, K.F, ROI, LOD, MP, Klarheit, Löslichkeit, mikrobieller Grenztest usw.
Proben? Bei den meisten Produkten werden kostenlose Muster zur Qualitätsbewertung bereitgestellt. Die Versandkosten müssen vom Kunden getragen werden.
Fabrikaudit? Werksaudit willkommen. Bitte vereinbaren Sie vorab einen Termin.
Mindestbestellmenge? Kein MOQ. Eine kleine Bestellung ist akzeptabel.
Lieferzeit? Wenn der Artikel vorrätig ist, ist die Lieferung innerhalb von drei Tagen garantiert.
Transport? Per Express (FedEx, DHL), auf dem Luftweg, auf dem Seeweg.
Dokumente? Kundendienst: COA, MOA, ROS, MSDS usw. können bereitgestellt werden.
Kundenspezifische Synthese? Kann maßgeschneiderte Synthesedienste anbieten, die Ihren Forschungsanforderungen am besten entsprechen.
Zahlungsbedingungen? Die Proforma-Rechnung wird Ihnen erst nach der Auftragsbestätigung zugesandt, unter Beifügung unserer Bankdaten. Zahlung per T/T (Telex-Überweisung), PayPal, Western Union usw.
Gefahrensymbole Xn - Schädlich
Risikocodes R40 - Es liegen begrenzte Hinweise auf eine krebserzeugende Wirkung vor
R36/37/38 - Reizt Augen, Atemwege und Haut.
R20/21/22 - Gesundheitsschädlich beim Einatmen, bei Berührung mit der Haut und beim Verschlucken.
Sicherheitsbeschreibung S22 - Staub nicht einatmen.
S36 - Tragen Sie geeignete Schutzkleidung.
S26 - Bei Augenkontakt sofort mit viel Wasser ausspülen und ärztlichen Rat einholen.
WGK Deutschland 3
RTECS TU3723000
HS-Code 2937 2900.99
Budesonid (CAS: 51333-22-3) (Markenname: Pulmicort) ist ein synthetisches Kortikosteroid-Medikament. Budesonid ist zur Erhaltung und prophylaktischen Behandlung von Asthma indiziert. Es wird auch zur Langzeitbehandlung chronisch obstruktiver Lungenerkrankungen (COPD) eingesetzt. Budesonid eignet sich auch zur Behandlung entzündlicher Darmerkrankungen, einschließlich Morbus Crohn, Colitis ulcerosa und mikroskopischer Colitis, sowie zur Behandlung von allergischer Rhinitis. Budesonid zeigt in vivo eine starke Glukokortikoidaktivität und eine schwache Mineralokortikoidaktivität. Es hemmt wirksam die Aktivitäten mehrerer Zelltypen und Mediatoren, die an allergischen oder nicht-allergischen Entzündungen beteiligt sind.
Budesonid ist ein in China häufig verwendetes klinisches Medikament zur Behandlung von Asthma bronchiale. Es kann bei nicht hormonabhängigem oder hormonabhängigem Asthma sowie bei chronischer asthmatischer Bronchitis eingesetzt werden. Oder es wird zur Behandlung von saisonaler allergischer Rhinitis und langjähriger allergischer Rhinitis eingesetzt und dient zur Verhinderung der Regeneration von Polypen nach der Entfernung von Nasenpolypen.