2021 Capecitabin von guter Qualität - Olaparib AZD-2281 CAS 763113-22-0 Reinheit ≥99,0 % API Factory – Ruifu
2021 Capecitabin von guter Qualität - Olaparib AZD-2281 CAS 763113-22-0 Reinheit ≥99,0 % API Factory – RuifuDetail:
Lieferung mit hochreiner, kommerzieller Produktion
| Chemischer Name | Olaparib |
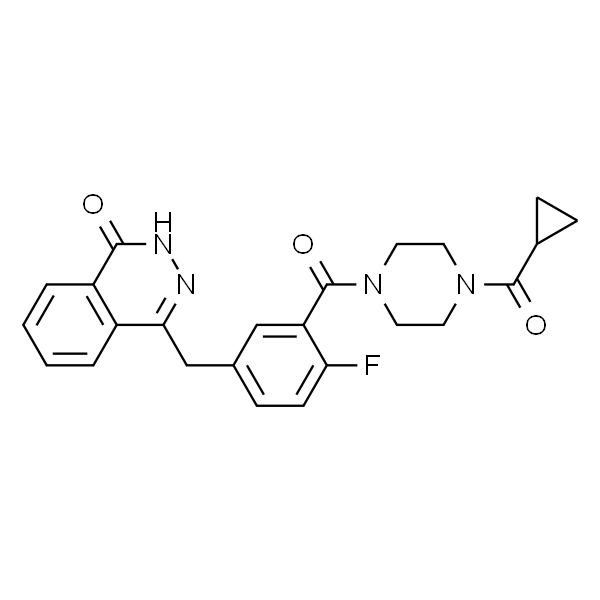
| Synonyme | AZD-2281; KU0059436; Lynparza; 4-(3-(4-(Cyclopropancarbonyl)piperazin-1-Carbonyl)-4-Fluorbenzyl)phthalazin-1(2H)-ein; 1-(Cyclopropylcarbonyl)-4-[5-[(3,4-dihydro-4-oxo-1-phthalazinyl)Methyl]-2-fluorbenzoyl]piperazin |
| CAS-Nummer | 763113-22-0 |
| CAT-Nummer | RF-API103 |
| Lagerstatus | Auf Lager, Produktionsmaßstab bis zu Hunderten von Kilogramm |
| Molekulare Formel | C24H23FN4O3 |
| Molekulargewicht | 434,46 |
| Löslichkeit | Löslich in DMSO |
| Marke | Ruifu Chemical |
| Artikel | Spezifikationen |
| Aussehen | Weißes bis cremefarbenes Pulver |
| Identifizierung durch 1H-NMR | Halten Sie sich an die Struktur |
| LC-MS | Halten Sie sich an die Struktur |
| Reinheit /Analysemethode | ≥99,0 % (durch LC-MS) |
| Feuchtigkeit (K.F) | ≤0,50 % |
| Einzelne Verunreinigung | ≤0,50 % |
| Gesamtverunreinigungen | ≤1,0 % |
| Schwermetalle (als Pb) | ≤20 ppm |
| Teststandard | Unternehmensstandard |
| Nutzung | API; PARP-Inhibitor |
Paket: Flasche, Aluminiumfolienbeutel, Papptrommel, 25 kg/Fass oder nach Kundenwunsch.
Lagerbedingungen:In verschlossenen Behältern kühl und trocken lagern; Vor Licht und Feuchtigkeit schützen.


Olaparib (CAS: 763113-22-0), ein hochwirksamer und selektiver PARP-Inhibitor. Am 19. Dezember 2014 genehmigte die FDA das neuartige Krebsmedikament Olaparib (Lynparza) als Monotherapie für Patientinnen mit fortgeschrittenem Eierstockkrebs, die sich mindestens drei Runden Chemotherapie unterzogen haben, oder für Patientinnen mit Verdacht auf BRCA-Mutationen. Gleichzeitig genehmigte die FDA die Quantifizierung und Klassifizierung von Diagnosekits zum Nachweis von Mutationen in BRCA1 und BRCA2, BRACAnalysis CDx. Olaparib ist das erste PARP-Inhibitor-Medikament, das von der FDA zugelassen wurde. Am 2. Februar 2015 genehmigte die Lebensmittel- und Arzneimittelbehörde der Europäischen Union (EMA) Olaparib auch für den Markteintritt in den 28 Ländern der Europäischen Union, darunter Island, Liechtenstein und Norwegen. Die Indikationen für die Zulassung durch die EMA und die FDA unterscheiden sich jedoch geringfügig. Ersteres gilt für Fälle von BRCA-Genmutationen und auch für die Erhaltungstherapie bei Patienten mit fortgeschrittenem epithelialem Eierstockkrebs, die zuvor platinhaltige Chemotherapeutika erhalten haben, darauf ansprechen und anfällig für ein erneutes Auftreten sind.
Produktdetailbilder:
Verwandter Produktführer:
Aufgrund unseres Spezialisierungs- und Reparaturbewusstseins hat sich unser Unternehmen bei Kunden auf der ganzen Welt einen hervorragenden Ruf für 2021 Capecitabin von guter Qualität - Olaparib AZD-2281 CAS 763113-22-0 Reinheit ≥99,0 % API-Fabrik – Ruifu, Das Produkt wird in die ganze Welt geliefert, beispielsweise nach Moldawien, Hyderabad, Pakistan. Wir integrieren alle unsere Vorteile, um unsere Industriestruktur und Produktleistung kontinuierlich zu erneuern, zu verbessern und zu optimieren. Wir werden immer daran glauben und daran arbeiten. Willkommen bei uns, um grünes Licht zu fördern. Gemeinsam werden wir eine bessere Zukunft schaffen!



